美国辉瑞的新冠疫苗和中国自主研发的新冠疫苗有何不同(组图)
2020年是新冠病毒(SARS-CoV-2)肆虐的一年,世界各地人民都经历了恐惧、担忧和绝望,各国政府也都在竭尽全力实现更多更快的检测,医护人员更是想方设法找到更快治愈病症的方法。人们不再能享受大型比赛的乐趣,也无法欣赏音乐艺术的美妙,更不能体会国际旅行的自由与便捷。
然而这一切的苦难似乎已经快要结束,美国的辉瑞(Pfizer)和德国的BioNTech两家生物制药公司宣布他们合作研发的疫苗在预防新冠肺炎(COVID-19)上达到了90%的有效性,大大超出了医学界对第一代新冠疫苗70%有效性的期望值。消息一出,金融市场反应剧烈,航空公司和电影公司等受疫情影响严重的产业股价接连上涨,辉瑞制药自己的股价更是在美股开盘时飙升15%。股市积极的反应代表了人们对渐渐趋向正常的生活充满了期待。
那么辉瑞的新冠疫苗和中国自主研发的新冠疫苗到底有何不同?目前各国研发的疫苗主要有三种技术路径,分别是:灭活疫苗、腺病毒载体疫苗、核酸疫苗。

中国的国药集团承担研发就是灭活疫苗,在11月6日第三届虹桥国际健康科技创新论坛上,国药集团董事长刘敬桢表示,目前已有包括中国国有企业驻外人员和留学生等在内的数十万人紧急接种了国药集团的新冠灭活疫苗,接种者中,没有一例不良反应,接种后离境人数达5.6万人,目前无一人感染。
灭活疫苗的技术路线即是在体外培养新冠病毒,然后将其灭活,丧失毒性,利用病毒的“尸体”刺激人体产生抗体,让免疫细胞记住病毒的长相。但是灭活疫苗免疫期短,国药集团的新冠疫苗预计只能产生六个月的抗体。另外灭活疫苗需要多次接种,且免疫途径单一,主要是体液免疫,缺少黏膜免疫,甚至造成抗体依赖性增强效应,反而使病毒感染更加严重。灭活疫苗的优点是技术相对成熟,易于保存。常见的狂犬、流感、百白破等疫苗都属于灭活技术路线。灭活疫苗的研发主要以人口大国为主,因为其更加实用,欧美国家没有押注这条技术路线,他们更倾向于技术前沿,如腺病毒载体和核酸疫苗的研发。
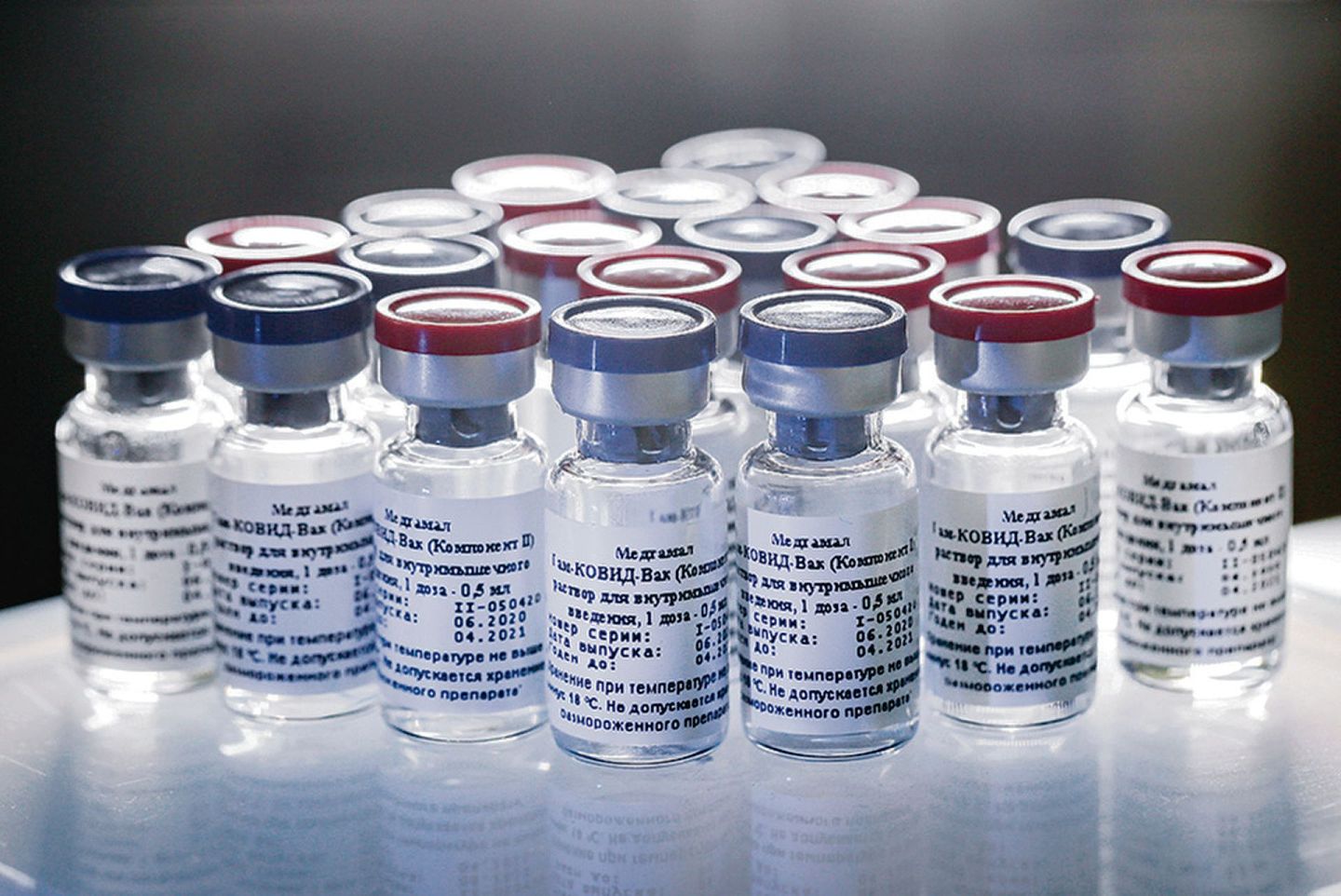
中国人民解放军军事医学研究院的陈薇院士研发的则是腺病毒载体疫苗,其作用原理是用经过改造后无害的腺病毒作为载体,装入新冠病毒的S蛋白基因,来刺激人体产生抗体。S蛋白是新冠病毒侵入人体所需的“小贼船”,无害的腺病毒坐着S蛋白的“小贼船”,佯装自己是坏人,让人体的免疫系统产生深刻印象。陈薇院士和天津康希诺生物技术有限公司联合自主研发的重组埃博拉病毒疫苗使用的就是腺病毒载体技术。
腺病毒载体疫苗理论上可以激活强烈的细胞免疫、体液免疫和黏膜免疫。但是因为腺病毒载体在人群中普遍易感,绝大多数人成长过程中都曾感染过不同的腺病毒,所以体内都存有能中和腺病毒载体的抗体,即“预存免疫”。“预存免疫”可能攻击载体,从而降低疫苗效果。英国的阿斯利康制药公司(AstraZeneca)和牛津大学合作研发的腺病毒疫苗在试验阶段曾导致志愿者死亡而一度中断试验。
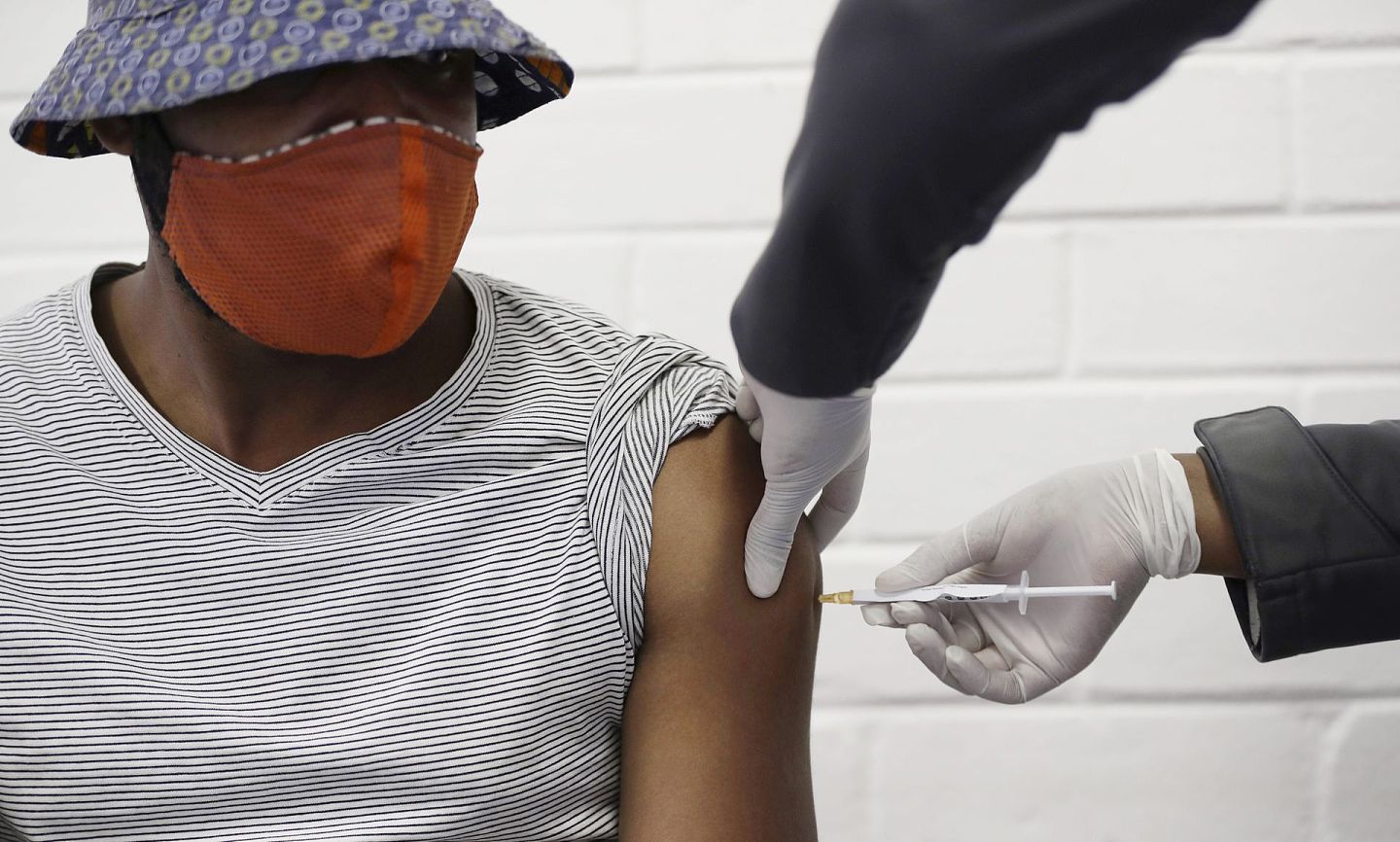
此次辉瑞的疫苗则是之前没有任何成功先例的核酸疫苗。核酸疫苗有DNA和mRNA两种,作用原理是将编码S蛋白的基因(DNA和mRNA)直接注入人体,利用人体细胞在体内合成S蛋白,从而刺激人体产生抗体。也就是说,把作业直接借给人体免疫系统抄。核酸疫苗目前是世界前沿技术,各国生物防御专家都在积极探索此技术,一旦成功,免疫效果将强劲且持久。但是因为成本昂贵,且需要在极低温环境下保存,很难在全球范围内普及。
总而言之,无论采取哪种技术路线,控制新冠肺炎大流行的各种疫苗距离上市已经指日可待。但是疫苗研制成功只是万里长征的第一步,目前为止全球并没有如此大规模疫苗接种的先例。联合国儿童基金会日前表态可以协助世界卫生组织联系各国冷冻链运输,以帮助各地区尽快获得疫苗。
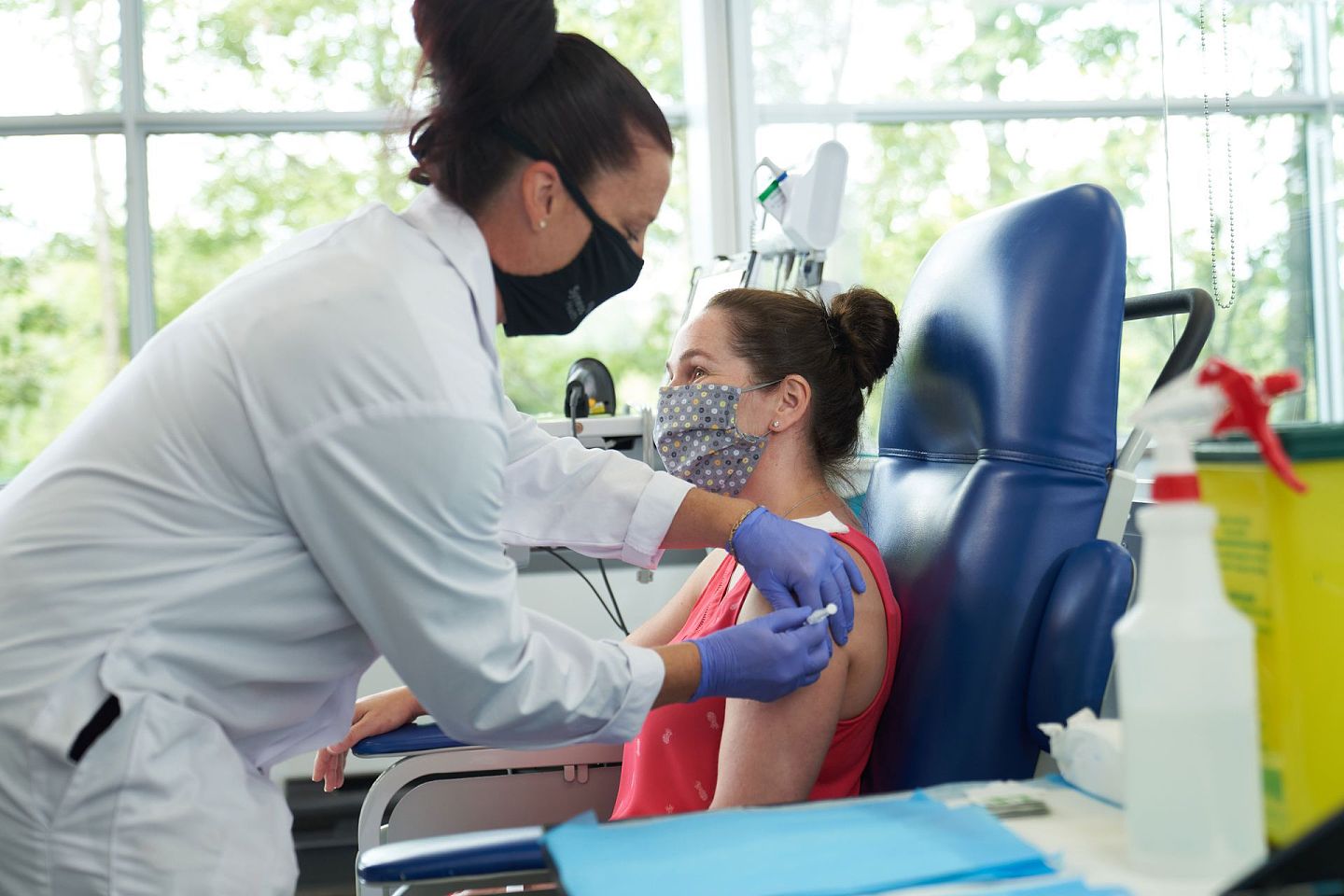
如果辉瑞的疫苗有效性确有90%,那么“群体免疫”将从理论变为现实,即便疫苗在生产初期并不能普及所有人口,但是只要有足够多的人群接种了疫苗,对未接种的人来说也是一个有效保护。
确定哪些地区和人群首先接种也将是个挑战,只有精准的锁定最易感人群,才能快速控制疫情,复苏经济。而新冠疫苗作为全球公共卫生产品,不应该沦落为国际政治博弈的砝码。毕竟病毒不分边境线,在各地区都解除危机前,没有任何人是绝对安全的。







 +61
+61 +86
+86 +886
+886 +852
+852 +853
+853 +64
+64


